אהרון בללו1*, אכדרי גיא2*, יבגני סמירנוב2*, אורית עמיר שגב2, הרשנהורן יוסף2, גלילי שמואל21 ודור ייבגניה2
1- המחלקה לגד"ש וירקות מכון וולקני.
2- המחלקה לעשבים נווה יער.
*- נחשבים ראשונים על המאמר
תקציר
המוטנט HRT1, העמיד לקוטלי עשבים מעכבי האנזים אצטולקטט סינתאז (ALS), התקבל באמצעות מוטגנזה כימית של זרעי עגבניות מזן M82. אפיון מולקולארי של המוטנט הראה שהעמידות נובעת ממוטציה נקודתית בגן המקודד לאנזים המטרה שגרמה להחלפה של חומצת אמינו אלנין לחומצת אמינו ולין. נערכו מחקרי חממה כדי לקבוע את תגובת הצמח כולו לקוטלי העשבים מקבוצות כימיות שונות. תוצאות ניסויים בחממה ובתנאי שדה הראו יעילות גבוהה של הדברת עלקת מצרית עם קוטלי העשבים קדרה ושוטגן. שני יישומים במינונים 0.966 או 1.44 גרם חומר פעיל לדונם או שלושה יישומים של 0.48 גרם חומר פעיל לדונם מנעו לחלוטין את הופעת גבעולי עלקת מצרית מעל פני הקרקע. שלושה וארבעה יישומים של אותם קוטלי עשבים בשדה במינון של 1.2 או 2.4 גרם חומר פעיל לדונם מנעו לחלוטין את הופעת גבעולי עלקת ללא כל הפסדי יבול גם בתנאי שדה.
מבוא
עמידות לקוטלי עשבים היא תכונה חשובה בגידולים חקלאים. רב הגידולים המסחריים העמידים לקוטלי עשבים נגזרו מהחלפה של נוקלאוטידים בודדים בגנים שיכולים להשתלב בזני עילית. גידולים עמידים לקוטלי עשבים מפותחים באמצעות טרנספורמציה של צמח עם גנים עמידים, מוטגנזה של זרעים, תרביות תאי צמחים או רקמות, ובאמצעות טכניקות גידול צמחים מסורתיות אחרות. מוטגנזה של זרעים היא גישה לא טרנסגנית, שנמצאה כאחת הגישות הכלכליות ביותר לקבלת עמידות לקוטלי עשבים בגידולים חקלאיים. לכן, שיטה זו שימשה בהצלחה לפיתוח זנים עמידים לקוטלי עשבים מעכבי האנזים אצטולקטט סינתאז (ALS) בגידולים מסחריים רבים(Rizwan and Akhtar, 2015) . שימוש נרחב בקוטלי עשבים מעכבי ALS הביא להופעת אוכלוסיות עשבים עמידות לקוטלי עשבים מסוג זה (Gaines et al., 2020; Owen et al., 2012). למרות זאת, קוטלי עשבים מעכבי ALS נותרו חשובים ברפרטואר קוטלי העשבים ההולך ופוחת, בשל טווח רחב של פעולות הדברה, רעילות נמוכה ליונקים, סלקטיביות גבוהה ופעילות גבוהה, מה שמאפשר שימוש במינונים נמוכים (Owen et al., 2012). בנוסף, עמידות לקוטלי עשבים מעכבי ALS הושגה באמצעות מוטגנזה בקווי גידולים רבים, כגון: תירס(Newhouse et al., 1991) , קנולה (Guo et al., 2022), אורזPiao et al., 2018) ), חיטה (Chen et al., 2021), שעורה(Lee et al., 2011) , חימצה (Galili et al., 2021) וכד'. קוטלי עשבים אלה פועלים על ידי עיכוב האנזים ALS שהוא אנזים מפתח במסלול הביוסינתטי של חומצות האמינו המסועפות לאוצין, איזולאוצין ו-ואלין. המחסור הנובע מחומצות אמינו אלו גורם למוות צמחים ALS .(Duggleby and Pang 2000; Owen et al., 2012) .ברוב המקרים, העמידות קשורה למוטציות בגנים המקודדים לתת היחידה הגדולה של האנזים ALS אשר גורמות להחלפה של חומצת אמינו שמורות באנזים Duggleby et al., 2008)).
צמחי עלקת הם צמחים טפילים שגורמים לנזקים חמורים ליבול ואיכותו בגידולים רבים, אך עיקר הבעיה בארץ מתמקדת בעלקת מצרית בעגבניות, המסכנת את קיומו של הענף (Dor et al., 2016). העלקת רגישה לקוטלי העשבים מעכבי ALS המשתייכים לשתי קבוצות כימיות (אימידזולינונים וסולפנילאוראות). בעוד שבתלתן ובאפונה ניתן להדביר בצורה יעילה עלקת עם אימידזולינונים פולסאר ופרסוט, בהתאמה, עגבנייה רגישה מאוד לאימידזולינונים. למרות שלצמחי העגבנייה יש סבילות לסולפונילאוראות, העמידות נובעת מפירוק שלהם לתוצרים לא רעילים באמצעות קומפלקס 450P, (Buker et al., 2004). לכן, הדברת עלקת עם סולפונילאוראות בצמחי עגבנייה דורשת הספקת קוטלי עשבים ישירות לצמחי העלקת. הדברה זו מבוססת על שלושה יישומים של מוניטור (Sulfosulfuron) כל פעם מלווה בהשקיה עילית של 30 קוב מים שמורידים את קוטלי העשבים אחרי הריסוס לקרקע ומשם הוא נקלט על ידי צמחי העלקת (Eizenberg et al., 2003, 2004, 2007; Hershenhorn et al., 1998a, 1998b). סטייה קלה מפרוטוקול מסובך זה, שעיתויו מבוסס על מודל ימי-מעלה, פוגעת באופן מהותי ביעילות ההדברה. לעומת זאת, מעכבי ALSשנקלטים דרך העלווה, מוסעים לשורש ונספגים אל תוך העלקת המהווה מבלע חזק וגורמים להדברתה (Dor et al., 2016, 2017)). האימידאזולינונים יעילים להדברת עלקת, והוכח כי ריסוס עלי שלהם כנגד טפיל זה דורש מינונים נמוכים יותר מאלה המשמשים להדברת עשבים ישירה. עם זאת, קוטלי עשבים אלה פוגעים במריסטמות הרבייה של צמחי עגבניות, ובמיוחד בפרחים ובניצני הפרי ומציבים מחסום לשימוש מסחרי נרחב (Eizenberg et al., 2008). לכן, באמצעות מוטגנזה כימית פיתחנו זן עגבנייה העמיד לקוטלי העשבים מקבוצת האימידזולינונים שקיבל שם 1HRT. בעבודה זו, איפינו את המוטציה שהביאה לעמידות במוטנט זה, ובחנו את האפשרות של שימוש במוטנט זה בהדברה כימית של עלקת מצרית.
חומרים ושיטות
חומר צמחי
החומר הצמחי בניסוי כלל זרעי זן העגבנייה M82 שתקבלו מחברת תרסיס וצמחי המוטנט העמיד HRT1 Dor et al., 2016)). זרעי עלקת נאספו מתפרחות של עלקת מצרית הטפילות על שורשי צמחי עגבניות שגדלו בקיבוץ בית השיטה. הזרעים אוחסנו בחדר קור ונשמרו בחושך בטמפרטורה של 4 מעלות צלזיוס עד לשימוש.
אפיון המוטציה לעמידות
גנום העגבנייה מכיל שלושה גנים של ALS הממוקמים על כרומוזומים 3, 6 ו-7 (Tomato Genome Consortium, 2012). כדי לקבוע את רצפי ה-DNA של שלושת גנים אלה הפקנו את כלל ה DNA הגנומי מעלים צעירים של צמחי M82 ו-HRT1 בשלב של 4 עלים אמתיים, כפי שתואר קודם לכן (Fulton et al., 1995). כל שלושת הגנים המקודדים לתת יחידה הגדולה של האנזים ALS בצמחי M82 ו-HRT1 הוגברו באמצעות ראקציית PCR, והמקטעים המוגברים רוצפו במעבדת Hylabs ברחובות. לקביעת המוטציה, רצפי ה-DNA של המקטעים המוגברים של כל גן ALS הושוו לרצפי הבר (WT) המתאימים להם שפורסמו על ידי Tomato Genome Consortium תוך שימוש בתוכנת DNAMAN 4.2 (Lynnon Biosoft, סן רמון, קליפורניה, ארה"ב).
בחינה של עמידות צולבת למעכבי ALS אחרים
בתנאי חממה נערכו שני ניסויים במתכונת בלוקים באקראי בחמש חזרות. זרעי M82 ו-HRT1 הונבטו במגשי חישתיל ו-4 שבועות לאחר הזריעה הועברו לעציצים בנפח 0.5 ליטר באדמת נווה יער. בשלב ארבעה עלים אמתיים, הצמחים רוססו במינונים הולכים וגדלים של קוטלי העשבים המצוינים בטבלה 1. צמחים שרוססו במים שימשו כחומרי בקרה. הנזק הצמחי הוערך ויזואלית על בסיס יומי במשך 21 ימים. בתנאי שדה הניסויי לבחינת העמידות של HRT1 לקוטלי עשבים קדרה נערכו בחוות גד"ש ובחוות עכו בחלקות נקיות מעלקת. הניסויים התבצעו במתכונת של בלוקים באקראי בארבע חזרות. כל חלקה כללה 12 מ"ר (אורך 6 מ' ורוחב 2 מ'). שתילי העגבניות נשתלו בשתי שורות במרחק של 40 ס"מ זו מזו עם מרחק של 35 ס"מ בין צמחים בכל שורה. חודש לאחר השתילה החלקות רוססו בקדרה במינונים של 0 (ביקורת), 2.4, 4.8, 7.2, 9.6 ו 14.4 גרם חומר פעיל לדונם. הערכה ויזואלית של הצמחים התבצעה אחת לשבועיים, בסוף הניסוי נשקלו כל העגבניות של כל חלקה לקביעת היבול.
טבלה 1. קוטלי עשבים ששימשו לבחינת עמידות צולבת.
שם מסחרי מינון (גרם חומר פעיל לדונם) חברה משווקת קדרה 0-14.4 לוכסמבורג שטוגן 0-3.8 אדמה אגן פולסאר 0-8.0 כצט סטייפל 0-6.8 גדות אגרו מוניטור 0-24 אדמה אגן אנווק 0-2.4 מכתשים אדמה גלין 0-6.8 גדות אגרו אקיפ 0-9.0 לידור אלמנטס אולימפוס 0-22.4 לידור אלמנטס
הדברת כימית של עלקת באמצעות קוטלי עשבים מעכבי ALS בתנאי חממה
זרעי M82 ו-HRT1 הונבטו במגשי חישתיל ו-4 שבועות לאחר הזריעה הועברו לעציצים בנפח 2.0 ליטר מלאים באדמת נווה יער מאולחים בזרעי עלקת בריכוז של 15 מ"ג זרעים לק"ג אדמה (כ-2,250 זרעים לק"ג אדמה). קוטל עשבים קדרה או שוטגן במינון של 0.48 גרם חומר פעיל לדונם יושם שלוש פעמים ב-230, 500 ו-690 ימי מעלה (GDD). גבעולי עלקת נספרו אחת לשבוע. הניסוי הסתיים 7 שבועות לאחר היישום האחרון של קוטל עשבים. השורשים נשטפו בעדינות מהעציץ ונספרו מספר הדבקות של עלקת על גבי השורשים.
הדברת כימית של עלקת באמצעות קוטלי עשבים מעכבי ALS בתנאי שדה
שני ניסוי הדברת העלקת נעשהו באותה מתכונת כמו ניסוי הפיטוטקסיות רק בחלקה הידועה כמאולחת מאד בזרעי עלקת מצרית. טמפרטורות הקרקע נרשמו מדי שעה לאורך עונת הגידול באמצעות אוגרי נתוני טמפרטורה שהוטמנו בעומק של 5 ס"מ במרכז חלקת הניסוי. צמחי עגבניות רוססו ארבע פעמים אחרי 190, 520, 880 ו-1,200 GDD בקדרה או שוטגן במינון עם 1.2 או 2.4 גרם חומר פעיל לדונם, בהתאמה. חלקות שלא טופלו שימשו כביקורות. הערכה חזותית של צמחי העגבניות בוצעה במרווחים של שבועיים. הפירות נאספו בנפרד מכל חלקה לקביעת היבול.
ניתוח סטטיסטי
התוצאות עברו ניתוח ANOVA באמצעות תוכנת JMP, גרסה 5.0 (SAS Institute Inc., Cary, NC). רגרסיות לא לינאריות עם Sigma-Plot גרסה 11.01 (SPSS Inc., Chicago, IL).
תוצאות ודיון
אפיון המוטציה לעמידות
ניתוח רצפי ה DNA של שלושת הגנים המקודדים ל ALS גילה מוטציה נקודתית של בסיס C לבסיס T בגןALS1 במיקום 581 (איור 1א) הממוקם על כרומוזום 3 (Tomato Genome Consortium 2012). מוטציה זו הביאה להחלפה של חומצת אמינו אלנין לחומצת אמינו ואלין בעמדה 194, התואם לעמדה 205 בצמחי ארבידופסיס (איור 1ב). מוטציה כזו נמצאה גם בצמחים אחרים העמידים למעכבי ALS מקבוצת האימידזולינונים כגון: חימצה (Thompson and Tar’an 2014), חמנית .(White et al., 2003) למיטב ידיעתנו, זהו הדיווח הראשון על מוטציה של אלנין ב-Val-194 (על פי Arabidopsis 205) בעגבניות המקנה עמידות לאימידזולינונים. לא נמצאו מוטציות נוספות בגן זה, או בשני הגנים ALS2 או ALS3 הממוקמים על כרומוזומים 7 ו-6, בהתאמה (נתונים לא מוצגים).

איור 1. ניתוח רצפים של הגן ALS1 המקודד לתת יחידה הגדולה של האנזים ALS הממוקם על כרומוזום 3. (א) רצפי בסיסי DNA (630–574) של ארבידופסיס (ARA) DNA (597–541) של הזן M82 ו-HRT1. המוטציה מבסיס C לבסיס T במיקום 581 (614 לפי ארבו ופסיס) מסומנת באדום . (ב) רצף חומצות אמינו (181-191) של תת יחידה הגדולה של האנזים ALS מעגבנייה מהזן M82 ומHRT1 המגבילים לרצף חומצות אמינו (202–192) בצמחי ארבידופסיס (ARA). המעבר מאלנין לואלין במיקום 194 (205 לפי ארבידופסיס) מסומן בתכלת.
עמידות של HRT1 למעכבי ALS בתנאי חממה
צמחי M82 היו מאד רגישים לכל מעכבי ALS מקבוצת האימדזולינונים שנבחנו. תסמיני נזק נצפו כבר במינון של 1.0 גרם חומר פעיל לדונם של פולסאר (איור 2א), ובמינון של 0.48 גרם חומר פעיל לדונם קדרה (איור 2ב). הנזק גדל עם העלייה במינון קוטל העשבים, כך שבמינון הגבוה ביותר, התפתחות הצמח הייתה רק 10% מצמחי הביקורת. לעומת זאת, צמחי HRT1 הראו סימני נזק בולטים רק במינונים הגבוהים ביותר של 8.0 ו-6.0 גרם חומר פעיל לדונם, מה שהפחית את התפתחות הצמח ל-65% ו-80% בהתאמה, מצמחי הביקורת (איור 2א,2ב). LD50 (מינון קוטל עשבים הגורם להפחתה של 50% בביומסה) אחרי ריסוס בקדרה בצמחי M82 היה כ 0.96 גרם חומר פעיל לדונם וכ- 8.0 גרם חומר פעיל לדונם בצמחי HRT1 (גבוה פי 24 מאשר עבור צמחי M82). תוצאות דומות התקבלו גם אחרי ריסוס בשוטגן (תוצאות לא מוצגות). LD50 של צמחי HRT1 אחרי ריסוס בפולסאר ושוטגן היה גבוה פי 14 ו 23 מצמחי M82, בהתאמה. רמות העמידות לאמידזולינונים שדווחו בצמחים עמידים אחרים נעות בין פי 4 ל-5 עבור חסה קוצנית (Mallory-Smith et al ., 1990), פי 30-50 בקו תירס 4522 (Anderson and Georgeson, 1989), ופי 200 בצמחי ארבידופסיס (Haughn and Somerville, 1990). עם זאת, השוואה אמתית ואובייקטיבית לנתונים בספרות כמעט בלתי אפשרית. כיון ששיטות יישום קוטלי עשבים, שלב הפנולוגי של הצמח בזמן יישום קוטל העשבים ופרמטרים כמו מצע גידול, גודל עציץ, טמפרטורה וכו' משפיעים על רמות העמידות/רגישות. רמת העמידות של צמחי HRT1 הייתה גבוה גם אחרי ריסוס בסטייפל השייך לקבוצת פיריטיובק סודיום (Pyrithiobac sodium). צמחי עגבניות M82 הראו עמידות גבוה אחרי ריסוס במוניטור ואנווק (מעכבי ALS ממשפחת הסולפונילאוראות). ירידה בהערכה הויזואלית נצפתה רק 5 ימים לאחר הטיפול מ-95% ל-80% עבור מוניטור ומ-95% ל-65% עבור אנווק, בהתאמה (נתונים שלא מוצגים). בסוף הניסוי, לא נצפו הבדלים חזותיים בין צמחי M82 וצמחי HRT1 שרוססו בשני חומרים אלה (נתונים לא מוצגים). לעומת זאת, גם צמחי M82 וגם צמחי HRT1 היו רגישים לקוטל העשבים אקיפ, השייך גם הוא לקבוצת הסולפונילאוריאות, (איור 2ג). צמחי M82 מתו 3 שבועות לאחר יישום של 4.5 ו-9.0 גרם חומר פעיל לדונם, בעוד שרק המינון הגבוה ביותר של 9.0 גרם חומר פעיל לדונם גרם לתמותה מוחלטת של צמחי HRT1. תוצאות אלה של עמידות שונה לסולפונילאוריאות בעגבנייה דומות לאלה שדווחו קודם לכן (Hershenhorn et al., 1998a,b, c; 2009). לכן, קוטלי עשבים מסוג סולפונילאוריאה מסוימים משמשים בהצלחה להדברת עלקת מצרית בעגבניות (Eizenberg et al., 2013). תוצאות דומות התקבלו גם בריסוס באולימפוס השייך לקבוצת ה Sulfonylamino-carbonyltriazolinone. גם צמחי M82 וגם צמחי HRT1 הראו עמידות גבוהה למינונים גבוהים של אולימפוס. גם כאן במינונים גבוהים יותר, HRT1 היה עמיד יותר מ-M82 (נתונים לא מוצגים).
עמידות של HRT1 לקדרה בתנאי שדה
נערכו שני ניסויי שדה לבחינת העמידות של צמחי HRT1 לקדרה. לא נמצאה שונות בין שני הניסויים לכן, ניתחנו את שני הניסויים ביחד. בשני הניסויים צמחי M82 היו רגישים מאד לריסוס בקדרה כבר במינון הנמוך ביותר (2.4 גרם חומר פעיל לדונם) M82 (טבלה 2א). בשני המינונים הנמוכים 2.4 ו 4.8 גרם חומר פעיל לדונם הנזק הוויזואלי פחת אחר 35 ו 42 ימים מהריסוס, בהתאמה, והצמחים לא נבדלו ויזואלית מצמחי הביקורת שלא רוססו. במינונים גבוהים יותר צמחי M82 לא התאוששו עד הקציר. מינון של 14.4 גרם חומר פעיל לדונם גרם לתמותה מוחלטת של צמחי M82. לעומת זאת, בצמחי HRT1 לריסוס קדרה לא הייתה השפעה נראית לעין על חיוניות, מראה או התפתחות הצמחים בכל המינונים שנבחנו למעט פגיעה קלה במינון 14.4 גרם חומר פעיל לדונם עד שבועיים מהריסוס (טבלה 2ב). בחוות עכו, יבול של צמחי M82 ו-HRT1 שלא טופלו הייתה כ-16 ו-13.8 טון דונם, בהתאמה. קדרה הפחית משמעותית את יבול של M82 (איור 3). מינונים של 2.4, 4.8 ו-7.2 גרם חומר פעיל לדונם הפחיתו את היבול לפחות מ-55%, 40% ו-13%, בהתאמה, מזו שנקטפה מחלקות הביקורת. במינונים של 9.6 ו-14.4 גרם חומר פעיל לדונם מנעו כמעט לחלוטין את היווצרות הפרי. יבול צמחי HRT1 לא הושפע מריסוס בקדרה באף אחד מהמינונים שנבדקו (איור 3) תוצאות דומות התקבל גם בחוות גד"ש למרות שהצמחים נשתלו מאוחר, ב-4 ביוני, והטמפרטורות בפריחה היו גבוהות ביותר, מעל 20 מעלות צלזיוס ברוב הלילות, שהביאו ליבול נמוך, כ-10 טון דונם עבור שני הזנים. בניסויים לבחינת העמידות, צמחי M82 שטופלו בקדרה במינון של 1.2 או 2.4 גרם חומר פעיל לדונם שלוש או ארבע פעמים במרווחים של כ-3 שבועות (סה"כ 3.6 עד 9.6 גרם חומר פעיל לדונם) לא שרדו, בעוד שבניסויים עם יישום אחד בלבד של 2.4, 4.8 ו-7.2 גרם חומר פעיל לדונם חלה ירידה ביבול אך הצמחים לא מתו (נתונים לא מוצגים).
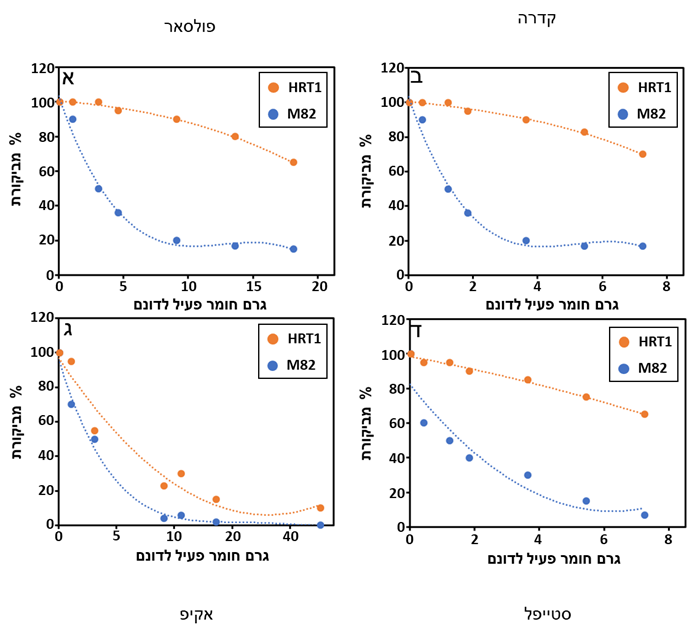
איור 2. השפעת ריסוס בפולסאר (א), קדרה (ב), אקיפ (ג) וסטייפל (ד) על הערכה ויזואלית של צמחי עגבנייה מהזן M82 וצמחי עגבנייה של המוטנט העמיד HRT1.
טבלה 2. הערכה ויזואלית (% מביקורת) בתנאי שדה של צמחי עגבנייה מזן M82 (א) והמוטנט HRT1 (ב) 7-42 ימים אחרי ריסוס בקדרה במינונים 0-14.4 גרם חומר פעיל/דונם.
מינון גרם חומר פעיל לדונם קו עגבנייה ימים מריסוס 0 2.4 4.8 7.2 9.6 14.4 א. M82 7 100a 63b 53bc 48c 35d 30d 14 100a 60b 53b 48b 25c 20c 21 100a 63b 50c 43c 30d 28d 28 100a 60b 48c 43c 25d 23d 35 100a 100a 73b 55b 30c 2.5d 42 100a 95a 95a 63b 50b 0c ב. HRT1 7 100a 100a 100a 93a 100a 85b 14 100a 100a 98a 100a 100a 90b 21 100a 100a 98a 100a 100a 100a 28 100a 100a 100a 100a 100a 100a 35 95a 100a 100a 98a 100a 100a 42 93a 100a 100a 100a 100a 100a
אותיות שונות בכל עמודה מצביאות על מובהקות סטטיסטית P≤0.05 כפי שהתקבל ממבחן t.
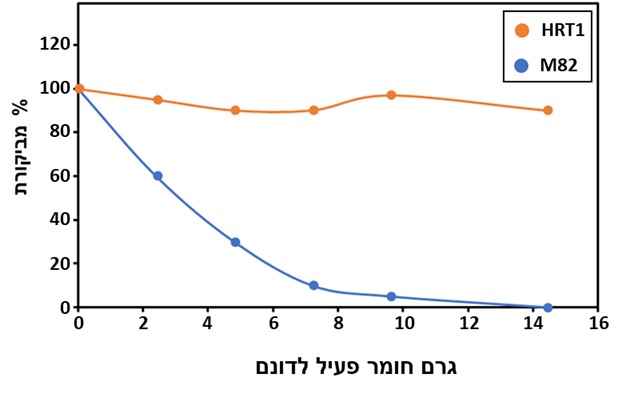
איור 3. השפעת מינון קדרה (גרם חומר פעיל לדונם) על יבול צמחי עגבנייה מהזן M82 ו המוטנט HRT1 בתנאי שדה. 100% בצמחי M82 היה שווה לכ- 16 טון/דונם בחוות עכו וכ- 10 טון לדונם בחוות גד"ש, וצמחי HRT1 לכ- 14 טון לדונם בחוות עכו ו 10 טון/דונם בחוות גד"ש.
הדברת עלקת מצרית במוטנט HRT1 בתנאי חממה
בסיום הניסוי, עציצי הביקורת הכילו שישה עד שמונה נבטי ? לכל צמח M82 או HRT1. צמחי M82 לא סבלו את טיפולי קוטלי העשבים ומתו. כל הטיפולים מנעו לחלוטין את צמיחת נבטי העלקת המצרית מעל הקרקע בעציצים עם צמחי HRT1. האדמה נשטפה בעדינות מהעציצים כדי לחשוף את השורשים, צמחי העלקת המצרית הופרדו מהשורשים ונשקלו. משקל צמחי העלקת המצרית בצמחי הביקורת M82 ו-HRT1 הגיעה ל-110 עד 120 גרם לצמח. קדרה במינון של 0.96 גרם חומר פעיל דונם שיושם פעמיים אחרי 230 ו-690 GDD או במינון של 0.48 גרם חומר פעיל לדונם שיושם שלוש פעמים אחרי 230, 500 ו-690 GDD הפחיתה את המשקל הטרי של צמחי העלקת המצרית פי 10 (10 עד 12 גרם לצמח) בהשוואה לצמחי הביקורת (איור 4). שני יישומים של 1.44 גרם חומר פעיל לדונם מנעו כמעט לחלוטין את טפילות צמח העלקת המצרית, עם ביומסה של כ-4 גרם עלקת מצרית לכל צמח עגבנייה. כל הטיפולים עם שוטגן הפחיתו משמעותית את הביומסה של צמח העלקת המצרית. שני יישומים של 0.96 גרם חומר פעיל לדונם או שלושה יישומים של 0.48 גרם חומר פעיל לדונם הפחיתו את הביומסה של העלקת המצרית לכ-34 ו-28 גרם, בהתאמה. שני יישומים של1.44 גרם חומר פעיל לדונם הפחיתו את הביומסה ל-13 גרם. קדרה ושוטגן מנעו את הופעת גבעולי הפריחה של העלקת המצרית מעל הקרקע, אך אין זה מוכיח שנמנע נזק לצמחי העגבניות. למעשה, רוב הנזק לפונדקאי מתרחש בשלב התת-קרקעי של הטפיל (Eizenberg et al., 2013). לכן, חיוני לשטוף את האדמה מהעציצים ולקבוע את המשקל הטרי של העלקת המצרית התת-קרקעית על השורשים. התוצאות הצביעו על כך ששני קוטלי העשבים לא רק מנעו לחלוטין את הופעת גבעולי עלקת מצרית מעל הקרקע, אלא גם הפחיתו משמעותית את הביומסה של צמח העלקת המצרית בתוך הקרקע. קדרה משמש בשדות עגבניות נגועים בצמח עלקת מצרית בישראל, עם יישום אחד או שניים של 0.5 עד 0.7 גרם חומר פעיל לדונם כל אחד לקראת סוף עונת הגידול, החל מכ-6 שבועות לפני הקטיף. מינון זה מיושם על צמחי עגבניות מפותחים לחלוטין ולא ניתן ליישם אותו מוקדם יותר בגלל השפעתו המזיקה על ניצנים, פרחים ולהתפתחות הפירות. בניסויי החממה שלנו, קוטלי עשבים יושמו מוקדם יותר על צמחים קטנים בהרבה, לא נצפה נזק לצמחי ה-HRT1, והושגה הפחתה מצוינת בביומסה של העלקת המצרית.
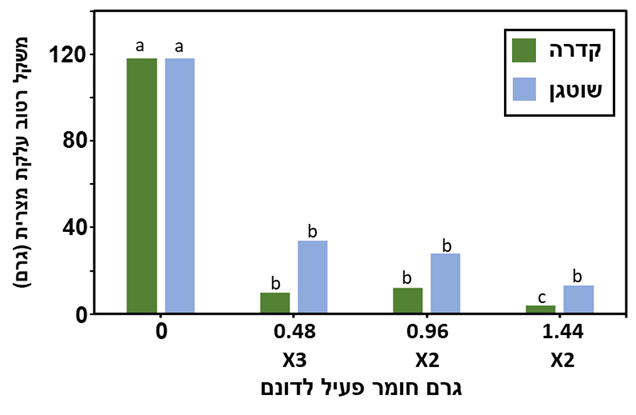
איור 4. השפעת ריסוס בקדרה ושטוגן על משקל רטוב של צמחי עלקת מצרית (גרם) בשורשי עגבנייה בתנאי חממה. מספר היישומים של קוטלי העשבים כתוב תחת המינון. אותיות שונות מציינות הבדלים מובהקים P≤0.05 כפי שהתקבל במבחן טוקי קרמר.
הדברת עלקת מצרית באמצעות HRT1 בתנאי שדה
כדי להעריך את יעילות הדברת עלקת מצרית עם צמחי HRT1 נערכו שני ניסויי שדה, האחד בחוות עכו והשני בחוות גד"ש בחלקות הידועות כמאולחות בעלקת מצרית. צמחי M82 לא שרדו את יישומי קוטלי עשבים ומתו, לכן מוצגות רק תוצאות של צמחי HRT1. מספר גבעולי עלקת מצרית שנספרו בחלקות הביקורת של HRT1 היה כ-80 עלקות למ"ר. למרות שקדרה ושוטגן שיושמו כל אחד בשלושה או ארבעה מועדים במינון של 1.2 או 2.4 גרם חומר פעיל לדונם, בהתאמה, לא ניתן היה לקבוע מינון אופטימאלי מכיוון שכל הטיפולים מנעו לחלוטין את התפתחות צמחי העלקת המצרית מעל הקרקע. חל עיכוב בהתפתחות הצמחים בחלקות הביקורת והם לא הצליחו להתאושש עד סוף הניסוי כתוצאה משיעור ההדבקה הגבוה של עלקת מצרית. האומדן החזותי של צמחים אלה עמד על כ-65%. הצמחים בחלקות שטופלו בקוטלי העשבים התפתחו היטב והיו במצב טוב עד סוף הניסויים. התפתחותם החזותית המשוערת נעה בין 90 ל-98%. מצב זה בא לידי ביטוי ביבול העגבניות בסוף הניסוי. בחלקות שטופלו ארבע פעמים ב-2.4 גרם חומר פעיל לדונם של קדרה או שוטגן היה גבוה בכ- 70% מיבול חלקות הביקורת (איור 5). ניתן להסיק כי הנזק שנצפה בצמחים בחלקות הביקורת נבע מצמחי העלקת המצרית. מסקנה זו מבוססת על ההתפתחות והיבול התקינים של הצמחים בחלקות המטופלות ועל ניסויים לבחינת העמידות שבוצעו בשדות שאינם מאולחים בעלקת מצרית.
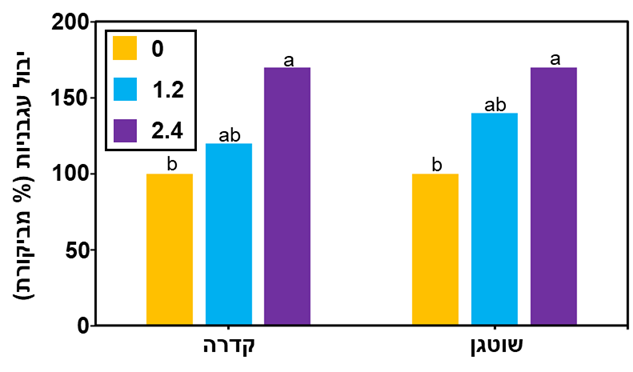
איור 5. השפעת ריסוס בקדרה או בשוטגן של צמחי עגבניות מקו HRT1 שגדלו בשדות מאולחים בעלקת מצרית על היבול. המינון של קוטלי העשבים מצוין בתוך הגרף. אותיות שונות מציינות הבדלים מובהקים P≤0.05 כפי שהתקבל במבחן טוקי קרמר.
לסיכום: בעונה זו איפינו מוטנט עגבנייה HRT1 העמיד לקוטלי עשבים מעכבי האנזים ALS. המוטנט הראה עמידות צולבת לקוטלי עשבים מעכבי האנזים ALS השייכים לקבוצות כימיות שונות, למעט סולפוניל אוריאות. הראנו ששימוש במוטנט זה יכול להיות כלי בהדברה כימית של עלקת תוך שימוש בקוטלי עשבים אלה.
מקורות
Anderson, P.C. and Georgeson, M., (1989). Herbicide-tolerant mutants of corn. Genome 31:994-999.
Buker, R. S., Rathinasabapathi, B., Stall, G. M., MacDonald, G. and Olson, S. M. (2004). Physiological basis for differential tolerance of tomato and pepper to rimsulfuron and halosulfuron: site action study. Weed Sci. 52:201–205.
Chen, Z., Wang, Z., Heng, Y., Li, J., Pei, J., Cao, Y., Deng, X. W. And Ma, L. (2021), Generation of a series of mutant lines resistant to imidazolinone by screening an EMS-based mutant library in common wheat. Crop J. 9:1030–1038.
Dor, E., Smirnov, E., Galili, S., Acadri, G., Hershenhorn, J. (2016). Characterization of the novel tomato mutant HRT, resistant to acetolactate synthase–inhibiting herbicides. Weed Sci. 64:348–360.
Dor, E., Galili, S., Smirnov, E., Hacham, Y., Amir, R. and Hershenhorn. J. (2017) The effects of herbicides targeting aromatic and branched chain amino acid biosynthesis support the presence of functional pathways in broomrape. Front Plant Sci. 8:707.
Duggleby, R. G., McCourt, J. A. and Guddat L. W. (2008). Structure and mechanism of inhibition of plant acetohydroxyacid synthase. Plant Physiol. Biochem. 46:309–324.
Duggleby, R. G. and Pang S. S. (2000). Acetohydroxyacid synthase. J. Biochem. Mol. Biol.33:1–36
Eizenberg, H., Hershenhorn, J., Graph, S. and Manor, H. (2003). Orobanche aegyptiaca control in tomato with sulfonylurea herbicides. Acta Hort. 613:205–208.
Eizenberg, H., Goldwasser, Y., Golan, S., Plakhine, D. and Hershenhorn, J. (2004) Egyptianbroomrape(Orobanche aegyptiaca Pers.) control in tomato with sulfonylurea herbicides—greenhouse studies. Weed Technol.18:490–496.
Eizenberg, H., Lande, T., Achdari,, G., Roichman, A. and Hershenhorn, J. (2007). Effect of Egyptian broomrape (Orobanche aegyptiaca) burial depth on parasitism dynamics and chemical control in tomato. Weed Sci.51:152–156.
Eizenberg, H., Hershenhorn, J., Ephrath, J. H and Kanampiu, F. (2013). Chemical control.
Pages 415–432 in Joel DM, Gressel, J. and Musselman LJ, eds. Parasitic Orobanchaceae: Parasitic Mechanisms and Control Strategies. New York, Heidelberg: Springer.
Gaines, T. A., Duke, S. O., Morran, S., Rigon, C. A. G., Tranel, P. J., Küpper, A. and Dayan, F. E. (2020). Mechanisms of evolved herbicide resistance. J. Biol. Chem. 295:10307–10330.
Galili, S., Hershenhorn, J., Edelman, M., Sobolev, V., Smirnov, E., Amir-Segev, O., Bellalou, A. and Dor, E. (2021). Novel mutation in the acetohydroxyacid synthase (AHAS), gene confers Imidazolinone resistance in chickpea Cicer arietinum L. plants. Plants 10:2791, 10.3390/plants10122791.
Guo, Y., Liu, C., Long, W., Gao, J., Zhang, J., Chen, S., Pu, H. anf Hu, M. (2022). Development and molecular analysis of a novel acetohydroxyacid synthase rapeseed mutant with high resistance to sulfonylurea herbicides. Crop J. 10:56–66.
Hershenhorn, J., Goldwasser, Y., Plakhine, D., Lavan, Y., Herzlinger, G., Golan, S., Chilf, T. and Kleifeld, Y, (1998a), Effect of sulfonylurea herbicides on Egyptian broomrape (Orobanche aegyptiaca) in tomato (Lycopersicon esculentum) under greenhouse conditions. Weed Technol. 12:115–120.
Hershenhorn, J., Plakhine, D., Goldwasser, Y., Westwood, J. H., Foy, C. L. and Kleifeld, Y, (1998b), Effect of sulfonylurea herbicides on early development of Egyptian broomrape (Orobanche aegyptiaca) in tomato (Lycopersicon esculentum). Weed Technol. 12:108–114.
Hershenhorn, J., Goldwasser, Y., Plakhine, D., Ali, R., Blumenfeld. T., Bucsbaum. H., Herzlinger, G., Golan, S., Chilf, T., Eizenberg, H., Dor, E. and Kleifeld, Y. (1998a). Orobanche aegyptiaca control in tomato fields with sulfonylurea herbicides. Weed Res. 38:343–349.
Hershenhorn, J., Eizenberg, H., Dor, E., Kapulnik, Y. and Goldwasser, Y, (2009,) Broomrape management in tomato. Weed Res, 49:34–47.
Lee, H., Rustgia, S., Kumara. N., Burkea, I., Yenisha, J. P., Gilla. K. S., Wettsteina, D. V. and Ullricha, S. E. (2011). Single nucleotide mutation in the barley acetohydroxy acid synthase (AHAS) gene confers resistance to imidazolinone herbicides PNAS 108: 8909–8913.
Mallory-Smith, C.A., Thill, D.C. and Dial, M.J. (1990). Identification of sulfonylurea herbicide-resistant prickly lettuce (Lactuca serriola). Weed Technol. 4:163-168.
Newhouse, K. E., Singh, B. K., Shaner, D. L. and Stidham, M. A. (1991). Mutations in corn (Zea mays L.) conferring resistance to imidazolinones. Theor. Appl. Genet. 83:65–70.
Owen, M. J., Goddin, D. E. and Powles, S. B. (2012). Identification of resistance to either paraquat or ALS-inhibiting herbicides in two Western Australian Hordeum leporinum biotypes. Pest Manag. Sci. 68:757–763.
Piao, Z., Wang, W., Wei, Y., Zonta, F., Wan, C., Bai, J., Wu, S., Wang, X. and Fang, J. (2018). Characterization of an acetohydroxy acid synthase mutant conferring tolerance to imidazolinone herbicides in rice (Oryza sativa). Planta 247:693–703.
Rizwan, M. and Akhtar, S. (2015). Development of herbicide resistant crops through induced mutations. Advancements in Life Sci. 3: 1-8.
The Tomato Genome Consortium. (2012). The tomato genome sequence provides insights into fleshy fruit evolution. Nature 485:635–641.
Thompson, C. and Tar’an, B. (2014). Genetic characterization of the acetohydroxyacid synthase (AHAS) gene responsible for resistance to imidazolinone in chickpea (Cicer arietinum L.). Theor. Appl. Genet. 127:1583–1591.
White, A. D., Graham, M. A. and Owen M. D. K. (2003). Isolation of acetolactate synthase homologs in common sunflower. Weed Sci. 51:845–853.












